
Vsa vsebina iLive je pregledana ali preverjena, da se zagotovi čim večja dejanska natančnost.
Imamo stroge smernice za pridobivanje virov in samo povezave do uglednih medijskih strani, akademskih raziskovalnih institucij in, kadar je to mogoče, medicinsko pregledanih študij. Upoštevajte, da so številke v oklepajih ([1], [2] itd.) Povezave, ki jih je mogoče klikniti na te študije.
Če menite, da je katera koli naša vsebina netočna, zastarela ali drugače vprašljiva, jo izberite in pritisnite Ctrl + Enter.
Umetna inteligenca zazna raka prostate v zgodnji fazi, ki ga patologi spregledajo
Zadnji pregled: 23.08.2025
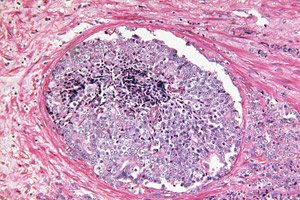 ">
">Znanstvena poročila dokazujejo, da lahko umetna inteligenca prepozna skrite morfološke sledi tumorja v biopsijah prostate, ki jih je patolog prej ocenil kot benigne. Model globokega učenja, usposobljen s šibko nadzorovanim pristopom, je napovedal, kateri moški s povišanim PSA bodo v naslednjih 30 mesecih razvili klinično pomembnega raka prostate (ISUP > 1) in kateri bodo ostali brez raka vsaj 8 let. To odpira vrata zgodnji stratifikaciji tveganja takoj po začetni »čisti« biopsiji in lahko pomaga pri odločitvi, kdo resnično potrebuje ponovne invazivne posege in okrepljen nadzor.
Ozadje študije
Primarna igelna biopsija prostate pogosto daje lažno negativne rezultate: znaten delež klinično pomembnega raka ostane »zunaj zaslona«, zlasti pri tradicionalni sistematični TRUS biopsiji. Uvedba MRI vodenja je povečala delež odkrivanja klinično pomembnega raka in zmanjšala število nepotrebnih ponovnih posegov, vendar tudi s sodobnimi strategijami nekateri agresivni tumorji ostanejo neodkriti. Klinična dilema ostaja enaka: koga je treba opazovati po »čisti« biopsiji in koga napotiti na zgodnjo ponovno biopsijo, da ne bi odložili diagnoze in bolnikov ne bi preobremenili z invazivnimi posegi.
Biološka osnova za rešitev tega problema je pojav TINT (tumor-instructed/indicating normal tissue): tumor »preoblikuje« okoliška na videz normalna tkiva organa in v njih pusti šibke, a sistematične sledi – od preoblikovanja strome in hipoksije do presnovnih premikov. Te spremembe so bile opisane v eksperimentalnih modelih in pri bolnikih z rakom prostate ter so povezane z agresivnostjo tumorja, zaradi česar je »normalno« tkivo potencialni vir diagnostičnih signalov, tudi če v biopsijskem jedru ni očitnih rakavih žlez.
Metode digitalne patologije in globokega učenja so namenjene ekstrakciji takšnih »subtilnih« značilnosti polja iz standardnih H&E rezov. Za razliko od klasične morfologije, ki se osredotoča na očitne tumorske strukture, lahko algoritmi zajamejo porazdeljene vzorce v stromi in epiteliju, povezane s prisotnostjo tumorja v drugem delu organa. To odpira pot do stratifikacije tveganja takoj po negativni biopsiji: visok »glassov rezultat« kaže na priporočljivost zgodnje ponovne biopsije ali vodenja z MRI, nizek pa podpira bolj nežno opazovanje.
To je ideja, na kateri temelji nova študija, objavljena v reviji Scientific Reports: avtorji so preizkusili, ali lahko umetna inteligenca napove klinično pomemben rak prostate v naslednjih 30 mesecih na podlagi morfoloških znakov iz biopsij TINT. Delo temelji na že predstavljenem preprintu in predstavlja uporabno osnovo za implementacijo "terenskih" digitalnih biomarkerjev pri usmerjanju pacientov po začetni "čisti" biopsiji.
Kako je bilo narejeno: zasnova, podatki, algoritem
Avtorji so retrospektivno zbrali kohorto 232 moških z zvišanim PSA in začetnim sklepom o "benignem" pri igelni biopsiji (po tehničnem nadzoru je bilo v končno analizo vključenih 213 bolnikov in 587 rezin; biopsije 1997–2016, Umea, Švedska). Vsak bolnik je bil po starosti, letu diagnoze in ravni PSA usklajen z "zrcalnim" parom: polovica je raka prostate diagnosticirala pozneje (≤30 mesecev), druga polovica pa je ostala brez raka vsaj 8 let. Preparati H&E so bili digitalizirani (20×), razrezani na ploščice velikosti 256 × 256 slikovnih pik in vneseni v CLAM (Clustering-constrained Attention Multiple-Instance Learning) – sodobno šibko nadzorovano shemo, kjer je znana le usoda bolnika in ne oznaka posameznega slikovnega piksla. Značilnosti je izluščil ResNet18, predhodno usposobljen na 57 naborih histopatoloških podatkov. Končna točka je binarna: nizko tveganje (benigno/ISUP1) v primerjavi z visokim tveganjem (ISUP2-5).
Natančnost napovedi
V neodvisnem testu je model dosegel AUC 0,81 na preparatih in AUC 0,82 na ravni pacienta. Pri pragu, ki je zagotavljal sprejemljivo ravnovesje, je bila občutljivost 0,92, stopnja lažno pozitivnih pa 0,32 (na ravni pacienta). Z drugimi besedami, med ljudmi, pri katerih je bila začetna biopsija »zgrešena«, je umetna inteligenca pravilno označila veliko večino tistih, pri katerih je bil kmalu potrjen klinično pomemben rak, čeprav za ceno nekaterih lažnih alarmov. Za kliniko je to signal: »benigni« odziv na biopsijo ≠ ničelno tveganje, in ga je mogoče kvantitativno stratificirati z digitalnim steklom.
Kaj točno umetna inteligenca "opazi" v "normalnem" tkivu?
Interpretacija prek UMAP in kart pozornosti je pokazala, da so stromalne spremembe najbolj informativne:
- Več kolagena v stromi (zbijanje matrice, »fibroza«);
- Manj gladkih mišičnih celic okoli žlez;
- Manj pogosti so subtilni signali v žleznem epiteliju, verjetno pod razpoložljivo ločljivostjo znižanja vzorčenja.
Ta vzorec se ujema s konceptom TINT (tumor-instructed/indicating normal tissue - tumor-navodila/oznaka normalnega tkiva): celo "norma" v organu, kjer je tumor skrit, se pod njegovim vplivom preoblikuje in se razlikuje od "norme" v organu brez tumorja. Rak ni le žarišče, ampak tudi polje, in umetna inteligenca se nauči brati učinek polja.
Kako je pristop uporaben v praksi – možni scenariji
- Ponovna biopsija na podlagi tveganja: visoka stopnja umetne inteligence na "čistem" steklu - argument v prid zgodnji ponovni biopsiji ali vodenju z MRI namesto čakanja.
- Prilagoditev spremljanja: Nizka hitrost uravnava tesnobo po »mejnem« slikanju z magnetno resonanco in omogoča zmernost intenzivnosti spremljanja.
- Usposabljanje za vzorec TINT: Zemljevidi pozornosti in interaktivni prekrivni elementi pomagajo patologom videti subtilna polja okoli raka, kar izboljša doslednost poročil.
Pomembno je razumeti omejitve
Gre za en sam center na severu Švedske (pretežno belo prebivalstvo), zasnova je retrospektivna, izhodiščne biopsije so bile opravljene brez nadzora MRI (sistematske TRUS biopsije), označevalci pa so prihodnji izidi in ne "prikriti tumor na istem preparatu". V neodvisnih centrih/skenerjih še ni zunanje validacije, prav tako ni prospektivnega preskušanja vpliva algoritma na klinične odločitve in izide. Stopnja lažno pozitivnih rezultatov ostaja pomembna – model ne nadomešča zdravnika, temveč dodaja verjetnostno plast za skupno odločanje.
Kaj sledi: Načrt izvajanja
- Večcentrična zunanja validacija (različni skenerji, protokoli, etnične skupine).
- Študije prospektivnih odločitev: ali rezultat umetne inteligence spremeni bolnikovo pot (čas do diagnoze, število nepotrebnih ponovnih biopsij, prekomerna/podcenjena diagnoza).
- Integracija z MRI in kliničnimi metodami: kombinirani modeli (PSA, MRI PIRADS, klinični dejavniki + TINT ocena po H&E).
- Tehnični koraki: standardizacija digitalizacije, nadzor nad odnašanjem podatkov, razložljivost (prekrivanje rutine s pozornostjo).
Vir: Chelebian E., Avenel C., Järemo H., Andersson P., Bergh A., Wählby C. in sod. Odkritje tumorja, ki kaže na morfološke spremembe v benignih biopsijah prostate, z umetno inteligenco. Znanstvena poročila (Nature Portfolio), objavljeno 21. avgusta 2025. DOI: https://doi.org/10.1038/s41598-025-15105-6
